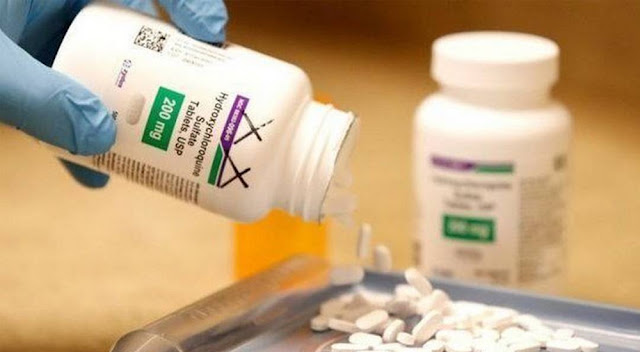
Desde a aprovação emergencial até hoje, o avanço das pesquisas trouxe evidências mais sólidas de que o remédio não contribui para a cura de infectados
A autorização para uso de cloroquina e hidroxicloroquina em caráter emergencial para pacientes com Covid-19 foi revogada pela FDA, a agência americana equivalente à Anvisa (Agência Nacional de Vigilância Sanitária), nesta segunda-feira.
A decisão da agência técnica governamental — que tem independência para seu funcionamento — vem apesar de o presidente americano Donald Trump ter promovido o uso do remédio contra o coronavírus.
Normalmente, o processo de aprovação do uso de um remédio pela FDA para uma nova doença é longo e contém muitas etapas. No entanto, diante da gravidade da pandemia, a agência havia autorizado o uso da cloroquina e derivados para tratar covid-19 em caráter emergencial, sem passar por todos os testes necessários, com base em estudos preliminares.
No entanto, desde a aprovação emergencial até hoje, o avanço das pesquisas trouxe evidências mais sólidas de que o remédio não gera melhora nos quadros de pessoas contaminadas pela doença.
A FDA diz que, com base na totalidade das evidências científicas disponíveis, não é mais razoável acreditar que o produto possa ser efetivo em tratar ou prevenir covid-19.
A agência diz também que não é mais possível considerar que os potenciais benefícios do remédio superam os riscos conhecidos e potenciais do seu uso. "É improvável o uso das duas substâncias tenha um efeito antiviral contra covid-19", diz.
Uma série de motivos foram listados pela agência como razões para a revogação da autorização:
- É improvável o uso das duas substâncias tenha um efeito antiviral contra covid-19
- Dados recentes de um estudo randomizado mostraram que não há diferença entre tratamento padrão e o uso de hidroxicloroquina e cloroquina
- As atuais recomendações de tratamento nos EUA já não incluem o uso dos remédios em pessoas hospitalizadas, tirando em casos de pesquisas clínicas
- Dados recentes de um grande estudo controlado e randomizado mostram que não há nenhum indício de que os remédios sejam capazes de prevenir a contaminação
- Cientistas não conseguiram reproduzir as primeiras observações feitas com os remédios que apontavam potenciais benefícios em ambientes controlados, com estudos clínicos randomizados.
A importância dos estudos clínicos
O que aponta se um remédio é realmente eficaz e seguro contra uma doença específica são pesquisas clínicas que seguem uma série de critérios, explica a bióloga Natália Pasternak, pesquisadora da USP e presidente do Instituto Questão de Ciência.
Estudos podem apontar que uma substância mata o vírus em laboratório, por exemplo, mas isso não significa que ela terá o mesmo efeito no corpo.
"O caminho normal da aprovação de um medicamento passa por um teste clínico controlado, randomizado, com duplo cego e com grupo placebo", diz Pasternak.
Isso tudo quer dizer que nesses estudos, um número grande de pessoas são divididas em grupos aleatoriamente, que recebem ou o remédio ou o placebo, e nem as pessoas nem os médicos que avaliam sua melhora sabem em qual grupo elas estão — essa informação é disponível apenas para a equipe que analisando os resultados.
Os estudos preliminares considerados pela FDA para aprovação emergencial dos medicamentos não seguiram esses critérios, que são essenciais para determinar a eficácia e segurança real dos remédios, explica Pasternak.
"Foi escancarado, com uma série de trabalhos muito bem conduzidos, que os remédios não tem eficácia nenhuma. Diante nessas novas evidências, a FDA não poderia manter uma autorização de emergencial", afirma a bióloga.
O uso no Brasil
A Organização Mundial da Saúde (OMS) não reconhece nenhum medicamento ou vacina para a covid-19, mas alguns países vinham autorizando o uso da cloroquina em caráter emergencial.
No Brasil, o Ministério da Saúde mudou o protocolo para o uso de cloroquina e hidroxicloroquina em 20 de maio, após o presidente Jair Bolsonaro ter promovido o uso diversas vezes — a posição do presidente gerou até a saída do ex-ministro da saúde Nelson Teich, que discordava do uso amplo no Sistema Único de Saúde (SUS).
Até então, a pasta recomendava esses medicamentos apenas para casos graves, quando médico e paciente concordam com o tratamento. As novas regras ampliaram seu uso também para os casos leves no SUS, mantendo a necessidade de autorização.
O Comitê Científico e a Diretoria da Sociedade Brasileira de Imunologia divulgou um documento em que afirma que "que diferentes estudos mostram não haver benefícios para os pacientes que utilizaram hidroxicloroquina". Já o Conselho Federal de Medicina condiciona seu uso ao critério médico e consentimento do paciente.
BBC News Brasil
Coronavírus,Mundo